Vejledningen kan downloades i Word- eller PDF-format.
Her kan du se øvelsen gennemgået på video.
Video: Forsuring af verdenshavene.
Tidsforbrug
Den praktiske del tager under 30 minutter.
Teori
Du har sikkert hørt, at koncentrationen af CO2 stiger i atmosfæren. Ligesom mange andre gasser kan CO2 opløses i vand. Fordi der samtidig er en ligevægt mellem CO2 i atmosfæren og CO2 i havet, betyder stigningen af CO2 i atmosfæren, at CO2-koncentrationen i havet stiger.
Spørgsmålet er, hvordan den ekstra CO2 påvirker pH-værdien i vand. Det skal I undersøge i laboratoriet.
Jeres udåndingsluft indeholder CO2, og derfor kan I efterligne den del af processen, hvor havet optager CO2 fra atmosfæren, ved at bruge et sugerør til at puste luft ned i et glas med vand.
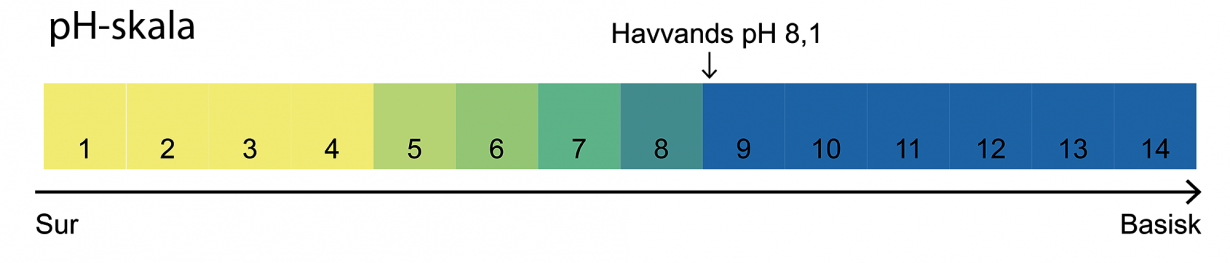
For at kunne se, om pH-værdien ændrer sig i vandet, er I nødt til at bruge en farveindikator, der kaldes bromthymolblåt og forkortes BTB. Når der sker ændringer i pH, skifter BTB farve. En væske, der er sur, bliver farvet gul, neutral væske bliver grøn, og basisk væske bliver blå.
Formål
I skal undersøge, hvordan CO2 fra luften, der er blevet opløst i vand, kan påvirke pH-værdien.
Materialer
-
1 reagensglas
-
1 sugerør
-
BTB-opløsning
-
Vand
Fremgangsmåde
-
Tilsæt 3 mL vand til et reagensglas.
-
Tilsæt 2 dråber BTB eller mere, hvis farven ikke er tydelig.
-
Pust i væsken i reagensglasset med et sugerør, til der sker et farveskift.
Diskussion
a) Forklar på baggrund af den observerede farveændring, hvordan CO2 påvirker pH-værdien i vand.
b) Hvilke konsekvenser kan øget koncentration af CO2 i havvand have for skaldyr?